СОДЕРЖАНИЕ
Липиды
Липиды (от греч. lipos – жир) – обязательный компонент любой живой клетки.
В клетках липиды представлены в виде жиров, восков, стероидных липидов (например, холестерин, витамин D), терпенов (ростовые вещества – гиббереллины, каротиноиды, витамин K), фосфолипидов, гликолипидов и липопротеидов. Это сложные эфиры, образованные жирными кислотами и трехатомным спиртом (глицерином). Карбоновые, или жирные, кислоты – небольшие молекулы с длинной цепью, состоящей из 16 или 18 атомов углерода, имеющие карбоксильную группу (–COOH) на одном из концов.
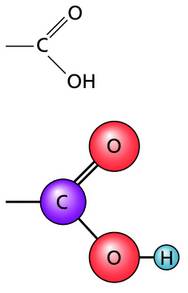 Модель и формула карбоксильной группы
Модель и формула карбоксильной группы
Жирные кислоты, имеющие одну двойную связь или более, называют ненасыщенными, не имеющие двойных связей – насыщенными кислотами. В зависимости от наличия простых или двойных связей в цепях жирных кислот проявляются физико-химические свойства жиров. Большинство жиров, в состав которых входят жирные кислоты с длинными насыщенными цепями, имеют при комнатной температуре твердую консистенцию, а с ненасыщенными – жидкую. Насыщенными жирными кислотами являются, например, стеариновая (C17H35COOH), пальмитиновая (C15H31COOH), ненасыщенными – олеиновая (C17H33COOH), линолевая (C17H31COOH) и линоленовая (C17H29COOH).
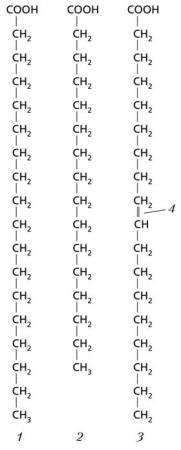 Карбоновые кислоты с длинными углеводородными цепями: 1 – стеариновая кислота (C18); 2 – пальмитиновая кислота (C16); 3 – олеиновая кислота (C18); 4 – участок с двойной связью
Карбоновые кислоты с длинными углеводородными цепями: 1 – стеариновая кислота (C18); 2 – пальмитиновая кислота (C16); 3 – олеиновая кислота (C18); 4 – участок с двойной связью
К наиболее распространенным липидам относятся нейтральные жиры. Нейтральные жиры в живых организмах являются энергетическим резервом (жир). Воска выполняют защитную функцию, покрывая прочным водонепроницаемым слоем клетки эпидермиса листьев, семян, плодов растений, а также кожу, перья и шерсть животных.
Фосфолипиды, или фосфатиды, – сложные липиды, в молекулах которых присутствует остаток фосфорной кислоты. В их состав входят насыщенные и ненасыщенные жирные кислоты. Структурная формула фосфолипида имеет гидрофильную головку, состоящую из глицерина, соединенного с холином (серином или др.), и двух жирных кислот, имеющих длинные хвосты. Фосфолипиды образуют самоорганизующиеся липидные бислои, составляющие основу всех клеточных мембран.
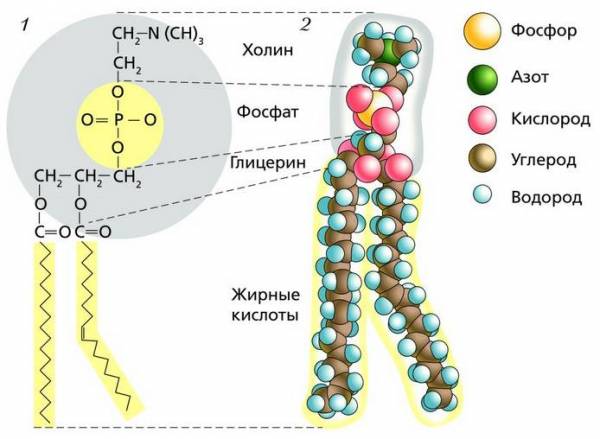 Строение фосфолипида: 1 – структурная формула; 2 – пространственная модель Стероиды – это липиды, относящиеся к классу изопренов, обладающих большой биорегуляторной активностью. К стероидам относят ряд гормонов (альдостерон, кортикостерон, тестостерон и др.), витамин D, феромоны, а также холестерин – компонент плазматической мембраны, ростовые вещества (например, гиббереллины).
Строение фосфолипида: 1 – структурная формула; 2 – пространственная модель Стероиды – это липиды, относящиеся к классу изопренов, обладающих большой биорегуляторной активностью. К стероидам относят ряд гормонов (альдостерон, кортикостерон, тестостерон и др.), витамин D, феромоны, а также холестерин – компонент плазматической мембраны, ростовые вещества (например, гиббереллины).
Биологическая роль липидов
Биологическая роль липидов разнообразна. Фосфолипиды составляют основу клеточной мембраны. Они определяют проницаемость мембран и активность многих ферментов. Энергетическая функция– также важное свойство липидов. Например, при полном окислении 1 г жира освобождается 38,9 кДж энергии, необходимой клетке. Запасание питательных веществ в виде жиров оказывается наиболее энергетически выгодным. Липиды могут быть твердыми (жиры животного происхождения) и жидкими (масла в клетках растений). Жир плохо проводит тепло, поэтому, например, у многих животных подкожная жировая прослойка не только служит источником питательных веществ и энергии, но и обеспечивает поддержание температуры тела, защиту органов от механических повреждений.
Белки, или протеины
Молекулы белков – полимеры, мономерами которых выступают аминокислоты, связанные между собой пептидной (или амидной) связью
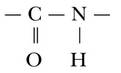 Пептидная связь Аминокислоты – это органические соединения, имеющие в своем составе карбоксильную группу (COOH) и одну или две аминогруппы (NH2). Кроме карбоксильной и аминогрупп, в молекуле аминокислот могут присутствовать радикалы (R), по которым их отличают друг от друга.
Пептидная связь Аминокислоты – это органические соединения, имеющие в своем составе карбоксильную группу (COOH) и одну или две аминогруппы (NH2). Кроме карбоксильной и аминогрупп, в молекуле аминокислот могут присутствовать радикалы (R), по которым их отличают друг от друга.
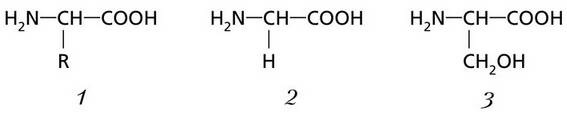 Формулы аминокислот: 1 – общая формула аминокислоты, где R – органический радикал; 2 – глицин; 3 – серин
Формулы аминокислот: 1 – общая формула аминокислоты, где R – органический радикал; 2 – глицин; 3 – серин
Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде. Из-за наличия карбоксильных и аминогрупп аминокислоты проявляют свойства как оснований, так и кислот. В природе насчитывается более 170 аминокислот, все они (кроме глицина, или аминоуксусной кислоты) могут существовать в виде двух оптических изомеров – D и L. В составе белков живых клеток встречаются только 20 аминокислот, все они образованы L-изомерами.
Все белки, имеющиеся в клетках, состоят только из L-аминокислот.
Растения и большая часть микроорганизмов способны самостоятельно производить весь набор аминокислот, необходимых для построения белковых молекул. В организме человека и животных восемь аминокислот не синтезируются и должны поступать с пищей. Такие аминокислоты называют незаменимыми. К ним относят валин, лейцин, изолейцин, лизин, метионин, треонин, триптофан и фенилаланин.
Важнейшее биологическое значение аминокислот состоит в том, что, являясь мономерами, они образуют полимерные цепи полипептидов и белков. Полипептидами называют полимеры, включающие до нескольких десятков аминокислот, тогда как белки содержат от ста до нескольких тысяч аминокислотных остатков.
Белки, или протеины, имеют большое значение в жизнедеятельности клеток любого организма. Поверхностный комплекс клетки, все ее внутренние структуры (цитоскелет) построены с участием белковых молекул. Ферменты (энзимы) – белки, принимающие участие во всех процессах жизнедеятельности и ускоряющие химические реакции. Они из всех органических веществ составляют наибольшую массу в клетке (50–70 %).
Длинная цепочка молекулы белка, состоящая из аминокислот, представляет собой первичную структуру белка. Она отображает химическую формулу белка. Полипептидная цепь обычно закручивается в спираль (вторичная структура белка), затем спираль еще скручивается, образуя комочек – глобулу (третичная структура белка). Несколько третичных структур, объединяясь между собой, могут создавать четвертичную структуру белка. Например, молекула гемоглобина состоит из четырех сложным образом свернутых полипептидных цепей. Четвертичная структура обычно наблюдается у сложных белков, состоящих из двух и более полипептидных цепей.
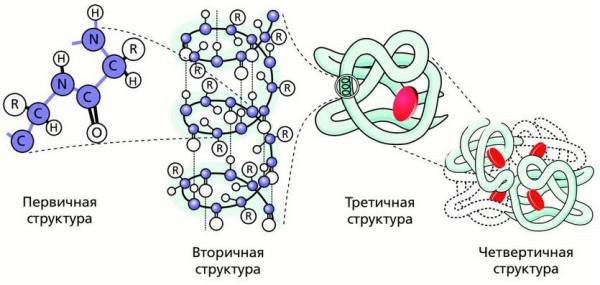 Структурная организация белка в молекуле гемоглобина
Структурная организация белка в молекуле гемоглобина
Таким образом, в строении молекулы белка наблюдаются различные структурные уровни организации. Первичная структура – цепь, вторичная структура – спираль, третичная структура – глобула. Первичная структура поддерживается прочными ковалентными связями. Вторичная структура возникает путем образования связей между NH- и CO-группами, находящимися при пептидной связи разных аминокислот. Третичная структура определяется преимущественно водородными связями между радикалами, а также дисульфидными мостиками (–S–S–), образующимися между серосодержащими аминокислотами.
При нарушении структуры белка, например при нагревании или химическом воздействии, он теряет свои качества и раскручивается – происходит его денатурация. Если денатурация затронула лишь третичную или вторичную структуру, то она обратима. Молекула белка может снова свернуться в спираль и уложиться в третичную структуру (ренатурация). При этом функции белка восстанавливаются. Это важнейшее свойство белков лежит в основе раздражимости живых систем, то есть способности клеток реагировать на внешние или внутренние раздражители.
Многообразие белков
В зависимости от формы белковой молекулы различают фибриллярные и глобулярные белки. Фибриллярные белки выполняют преимущественно опорную или защитную функцию, а глобулярные – динамическую функцию в клетке. К глобулярным белкам относят ферменты, некоторые гормоны и многие транспортные белки.
В зависимости от состава различают простые белки – протеины (состоят только из аминокислот) и сложные – протеиды, которые наряду с аминокислотами содержат углеводы, липиды, нуклеиновые кислоты, металлы и т. д.
Белки в клетках постоянно обновляются. Необходимость их постоянного обновления лежит в основе обмена веществ.
Функции белков
Функции белков в клетке очень разнообразны. Они участвуют во всех процессах ее жизнедеятельности. Входя в состав клеточных структур, они выполняют строительную (пластическую) функцию, обеспечивают транспорт веществ внутри клетки и между клетками. Специальные белки (миозин, актин) осуществляют движение клеток. Белки образуют антитела, которые наряду с регуляторными выполняют и защитные функции. Белки гистоны входят в состав хромосом. Но особенно важную роль в живой материи выполняют белки-ферменты (от лат. fermentum – брожение, закваска).
Ферменты – это особые белковые молекулы, ускоряющие химические реакции. Одни ферменты участвуют в реакциях синтеза, а другие – в реакциях распада. Обычно, для того чтобы превратить исходное вещество через ряд промежуточных соединений в «продукт», несколько ферментов действуют последовательно один за другим. Реакции протекают согласовано, подчиняясь строгой регуляции, что объясняется специфической природой ферментов. При этом один фермент катализирует всегда только одну реакцию. Последовательность реакций составляет так называемый метаболический путь. В клетке работает одновременно огромное число метаболических путей. Благодаря ферментам все биохимические процессы в клетке Идут в упорядоченном виде.
Белки – важнейшие биологические молекулы, без которых жизнь невозможна.