Стадии клеточного дыхания
У большинства эукариотических клеток процесс энергетического обмена не останавливается на гликолизе, и трехуглеродное соединение (пируват) вовлекается в дальнейшее окисление, происходящее с участием кислорода в митохондриях.
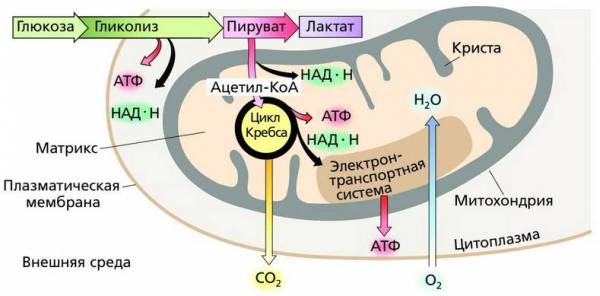 Взаимосвязь бескислородного и кислородного этапов энергетического обмена
Взаимосвязь бескислородного и кислородного этапов энергетического обмена
В отличие от гликолиза, кислородный этап энергетического обмена является мембранозависимым. Он происходит в матриксе митохондрий и на внутренних мембранах митохондриальных крист. Окислительные процессы в митохондриях начинаются сразу, как только пируват проникает в них.
Попав в матрикс митохондрии, пируват вступает на путь окислительного расщепления при участии пируватдегидрогеназного многоферментного комплекса, включающего разнообразные ферменты и коферменты. Этот комплекс отщепляет от пирувата атом углерода (он удаляется в виде CO2). Образовавшаяся двухуглеродная ацетильная группа (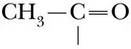 ) вступает в реакцию с серосодержащим коферментом A, или коэнзимом A (КоA). В итоге образуется соединение, которое называют ацетилкоэнзимом A или ацетил-КоA (HS-КоA). Во всех последующих реакциях окисления участвует не сам пируват, а его активированное производное – ацетил-КоA. Этот процесс представлен на рисунке.
) вступает в реакцию с серосодержащим коферментом A, или коэнзимом A (КоA). В итоге образуется соединение, которое называют ацетилкоэнзимом A или ацетил-КоA (HS-КоA). Во всех последующих реакциях окисления участвует не сам пируват, а его активированное производное – ацетил-КоA. Этот процесс представлен на рисунке.
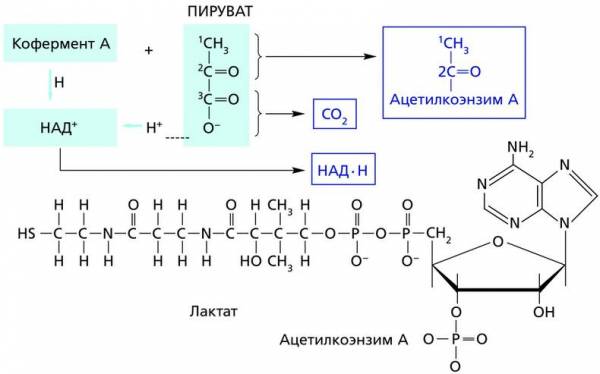 Схема подготовительного этапа, в котором из пирувата образуется ацетил-КоA
Схема подготовительного этапа, в котором из пирувата образуется ацетил-КоA
В митохондрии – в матриксе и на окружающей его внутренней мембране – происходит полное окисление пирувата до конечных продуктов CO2 и H2O. Из-за особенностей протекания этого процесса различают две его стадии: 1) цикл трикарбоновых кислот (цикл Кребса, или цикл лимонной кислоты) и 2) перенос электронов дыхательной цепью, где синтезируется АТФ. Рассмотрим кратко обе стадии кислородного этапа биологического окисления.
Цикл Кребса
Цикл трикарбоновых кислот (цикл Кребса, цикл лимонной кислоты) – центральная часть общего пути энергетического обмена, циклический биохимический аэробный процесс, в ходе которого происходит полное сгорание двух- и трехуглеродных соединений, образующихся в живых организмах как промежуточные продукты при распаде углеводов, жиров и белков до CO2. При этом освобожденный водород направляется в цепь тканевого дыхания, где в дальнейшем окисляется до воды, принимая непосредственное участие в синтезе универсального источника энергии – АТФ.
Цикл трикарбоновых кислот в живых клетках был открыт и изучен немецким биохимиком Гансом Кребсом (1937), за эту работу он (совместно с Фрицем Альбертом Липманом) был удостоен Нобелевской премии (1953).
У эукариот все реакции цикла Кребса протекают внутри митохондрий, причем катализирующие их ферменты, кроме одного, находятся в свободном состоянии в митохондриальном матриксе. Исключение составляет сукцинатдегидрогеназа (СДГ), которая локализуется на внутренней митохондриальной мембране, встраиваясь в липидный бислой. У прокариот реакции цикла протекают в цитоплазме.
Образовавшийся в митохондриях ацетил-КоA вступает в цикл Кребса, состоящий из восьми последовательно идущих друг за другом реакций. Начинается цикл с взаимодействия ацетил-КоA и четырехуглеродной щавелевоуксусной кислоты (ЩУК, оксалоацетата), в результате чего образуется лимонная кислота (цитрат). По этой причине цикл и получил свое название. Затем лимонная кислота (шестиуглеродное соединение) в результате ряда дегидрирований (отнятия водорода) и двух декарбоксилирований (отщепления CO2) теряет два углеродных атома и снова в цикле Кребса превращается в щавелевоуксусную кислоту – четырехуглеродное соединение, которое вновь взаимодействует с очередной молекулой ацетил-КоA, и цикл повторяется. Таким образом, в результате полного оборота цикла одна молекула ацетил-КоA сгорает до CO2 и H2O, а молекула оксалоацетата регенерируется.
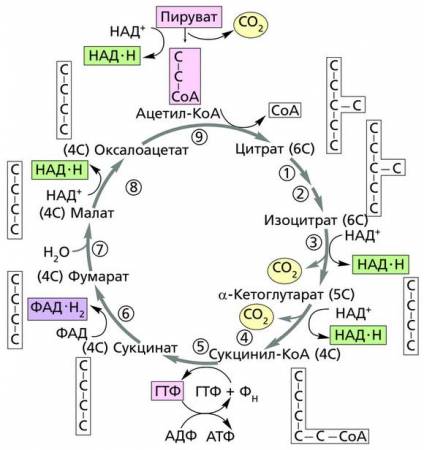 Цикл Кребса
Цикл Кребса
Первая реакция катализируется ферментом цитрат-синтазой, при этом ацетильная группа ацетил-КоA конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота (цитрат).
В результате второй реакции образовавшаяся лимонная кислота подвергается дегидратированию (отщепление воды) с образованием цис-аконитовой кислоты (цисаконитата), которая, присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат). Катализирует эти обратимые реакции гидратации-дегидратации фермент аконитатгидратаза (аконитаза). В результате происходит взаимоперемещение H + и OH — в молекуле цитрата.
В процессе третьей реакции изолимонная кислота дегидрируется в присутствии фермента НАД-зависимой изоцитратдегидрогеназы с образованием α-кетоглутаровой кислоты (α-кетоглутарата). В ходе изоцитратдегидрогеназной реакции изолимонная кислота одновременно декарбоксилируется. НАД-зависимая изоцитратдегидрогеназа является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ. Кроме того, фермент для проявления своей активности нуждается в ионах Mg 2+ или Mn 2+ .
Во время четвертой реакции происходит окислительное декарбоксилирование α-кетоглутаровой кислоты с образованием макроэргического соединения – сукцинил-КоA. Механизм этой реакции сходен с механизмом окислительного декарбоксилирования пирувата до ацетил-КоA, а α-кетоглутаратдегидрогеназный комплекс напоминает по своей структуре пируватдегидрогеназный комплекс. Как и в том, так и в другом случае в реакции принимают участие пять коферментов: ТПФ (тиаминпирофосфат), амид липоевой кислоты, HS-КоA, ФАД и НАД + .
Пятая реакция катализируется ферментом сукцинил-КоA-синтетазой. В ходе этой реакции сукцинил-КоA при участии ГДФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит обрзование макроэргической фосфатной связи ГТФ, что равносильно образованию одной молекулы АТФ.
Седьмая реакция катализируется ферментом фумаратгидратазой (фумаразой). Образовавшаяся фумаровая кислота (фумарат) гидратируется, продуктом реакции является яблочная кислота (L-малат).
Наконец, в ходе восьмой реакции цикла трикарбоновых кислот под действием митохондриальной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат.
Как видно, за один оборот цикла, состоящего из восьми ферментативных реакций, происходит полное окисление (сгорание) одной молекулы ацетата (ацетил-КоA).
Превращения ацетата можно представить суммарной реакцией:
Ацетил-КоA + ЗНАД + + ФАД + ГДФ + Фн + 2H2O → CO2 + ЗНАД·Н + ФАД·Н2 + ГТФ
Окисление химических связей в цикле Кребса сопровождается выделением энергии, которая потребляется несколькими способами. Так, в процессе пятой ферментативной реакции цикла синтезируется одна молекула макроэргического соединения – гуанозинтрифосфата (ГТФ). Кроме этого, в ходе других реакций (третьей, четвертой и восьмой) происходит высвобождение высокоэнергетических электронов, которые используются для восстановления молекул коферментов – переносчиков водорода – НАД + (никотинамидадениндинуклеотида) и ФАД (флавинадениндинуклеотида) в ходе шестой реакции цикла.
Поэтому в каждом обороте цикла Кребса три молекулы НАД + превращаются в три молекулы НАД·Н и одна молекула ФАД – в ФАД·H2.
Каждый оборот цикла дает две молекулы CO2, который диффундирует из митохондрий и покидает клетку.
Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА, а коферменты (НАД + и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. Это окисление осуществляется в системе переносчиков электронов в дыхательной цепи (цепи дыхательных ферментов), локализованной во внутренней мембране митохондрий.
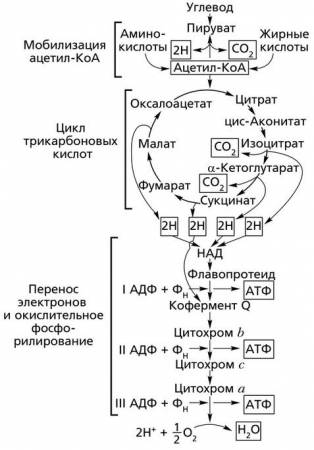 Схема кислородного этапа биологического окисления глюкозы
Схема кислородного этапа биологического окисления глюкозы
Таким образом, хотя в цикле Кребса не синтезируется АТФ, в нем происходят окисление молекул, перенос электронов на акцепторы, выделение CO2. В связи с этим цикл Кребса играет чрезвычайно важную роль в энергетическом обеспечении клетки. Он является тем центром, где сходятся все пути окисления ацетильных групп (в виде ацетил-КоА), в которые превращается в процессе диссимиляции большая часть органических молекул углеводов, аминокислот и жирных кислот. В ходе его реакций высвобождается основное количество энергии, содержащейся в окисляемом субстрате, причем большая часть энергии не теряется, а используется на заключительном этапе дыхательного процесса при образовании АТФ.
Цикл Кребса служит важным этапом окисления не только углеводов, но также белков, жиров и других органических соединений.
Однако следует помнить, что цикл Кребса функционирует только в условиях достаточного количества O2, хотя сам кислород не участвует в его реакциях. Кислород необходим для заключительного этапа – дыхательного процесса, связанного с окислением восстановленных молекул НАД·Н и ФАД·H2 во внутренней митохондриальной мембране.
Окислительное фосфорилирование
Окислительное фосфорилирование является последней стадией расщепления исходного субстрата (например, глюкозы), в ходе которого высвобождается значительное количество энергии, которая аккумулируется в макроэргических связях молекул АТФ. Окислительные реакции, обеспечивающие синтез АТФ, осуществляются во внутренней мембране митохондрий – в дыхательной цепи.
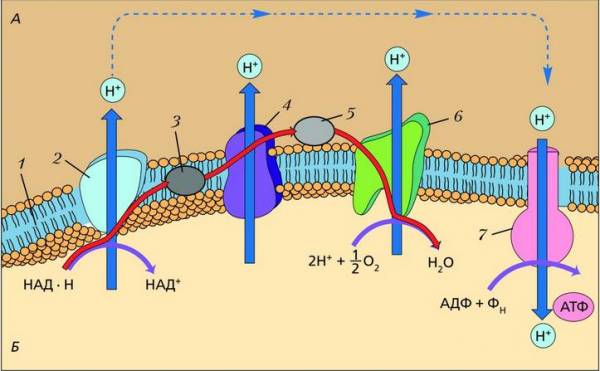 Перенос электронов через три ферментативных комплекса митохондрии от НАД·Н к O2 и синтез АТФ с использованием энергии резервуара H + : А – межмембранное пространство; Б – матрикс: 1 – внутренняя мембрана митохондрии; 2 – НАД·Н-дегидрогеназный комплекс; 3 – убихинон; 4 – комплекс (b–c1); 5 – цитохром C; б – цитрохромоксидазный комплекс; 7 – АТФ-синтаза. Красные стрелки – поток электронов (e — ), синие – поток протонов (H + )
Перенос электронов через три ферментативных комплекса митохондрии от НАД·Н к O2 и синтез АТФ с использованием энергии резервуара H + : А – межмембранное пространство; Б – матрикс: 1 – внутренняя мембрана митохондрии; 2 – НАД·Н-дегидрогеназный комплекс; 3 – убихинон; 4 – комплекс (b–c1); 5 – цитохром C; б – цитрохромоксидазный комплекс; 7 – АТФ-синтаза. Красные стрелки – поток электронов (e — ), синие – поток протонов (H + )
В митохондриальных мембранах размещаются не только ферменты- переносчики дыхательной цепи, но и фермент синтеза АТФ – АТФ-синтаза. АТФ-синтаза представляет собой белковый комплекс, состоящий из девяти субъединиц, по внешнему виду напоминающий гриб. АТФ-синтаза встроена во внутреннюю митохондриальную мембрану, обращенную в сторону матрикса, и сплошь пронизывает поверхность этой мембраны.
Высвободившиеся в процессе окисления в цикле Кребса электроны, акцептированные коферментами, переносятся в дыхательную цепь, представляющую собой ряд белковых комплексов, состоящих из ферментов и коферментов, локализованных на внутренней мембране митохондрий.
Транспорт электронов идет по дыхательной цепи от одного комплекса к другому. Среди них три особенно значимы для окисления субстрата. Вначале электроны НАД·H, синтезированного в цикле Кребса, поступают в первый комплекс с ферментом НАД·H-дегидрогеназой, который передает их на белок убихинон. Убихинон функционирует как переносчик и электронов, и протонов и переносит электроны на второй комплекс – убихинон-цитохром c1 с ферментом оксидоредуктазой, или (b-c-комплекс), который, в свою очередь, переносит их на третий (цитохромоксидазный) комплекс, откуда электроны передаются на кислород, в результате чего образуется вода. На этом окисление заканчивается, так как субстрат полностью расщепляется до CO2 и H2O.
Весь путь электронов в дыхательной цепи можно представить в виде схемы: НАД·H → НАД·H-дегидрогенизный комплекс → убихинон → комплекс цитохромов b-c1 → цитохром c → цитохромоксидазный комплекс – > молекулярный кислород. При этом пара электронов 3 раза пересекает мембрану.
На всех этапах перехода электронов с одного ферментного комплекса на другой окислительно-восстановительные процессы сопряжены с образованием молекул АТФ. Каким же образом энергия, запасенная в НАД·H и ФАД·H служит синтезу АТФ? Дело в том, что атомы водорода этих восстановленных соединений транспортируются в мембраны митохондрий, где они оставляют электроны (e-) на внутренней стороне мембран. Каждый белковый комплекс дыхательной цепи направляет энергию окисления на перемещение протонов (H+) через мембрану из матрикса в межмембранное пространство. В результате между наружной и внутренней поверхностью мембраны возникает разность потенциалов.
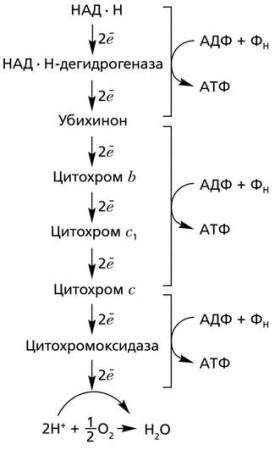 Упрощенная схема цепи переноса электронов и сопряженного с ней образования молекул АТФ
Упрощенная схема цепи переноса электронов и сопряженного с ней образования молекул АТФ 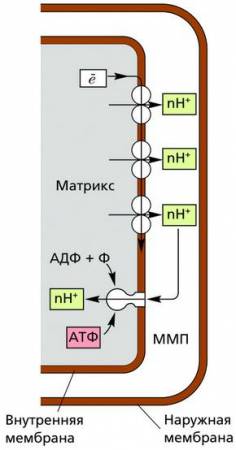 Накопление протонов в межмембранном пространстве митохондрий (ММП)
Накопление протонов в межмембранном пространстве митохондрий (ММП)
Когда электрохимический протонный градиент достигает критической величины (200 mW), белковый комплекс АТФ-синтазы, встроенный во внутреннюю мембрану митохондрий, начинает транспортировать протоны обратно в матрикс, при этом превращая одну форму энергии в другую: образует молекулы АТФ из молекул АДФ и неорганического фосфата (Фн). Таким образом, пока идет окисление субстрата и осуществляется перекачка протонов через внутреннюю митохондриальную мембрану, идет и сопряженный с ними синтез АТФ, то есть происходит процесс, называемый окислительным фосфорилированием.
Таким образом, окислительный процесс и окислительное фосфорилирование (синтез АТФ) – это два разных, но сопряженных процесса, происходящих в дыхательной цепи на внутренней митохондриальной мембране.
Впервые идею о сопряженности процессов окисления и фосфорилирования АДФ с образованием АТФ высказал в 1931 году российский биохимик, академик Владимир Александрович Энгельгардт.
Но сам механизм синтеза АТФ в реакциях фосфорилирования, сопряженного с биологическим окислением, процесс образования электрохимического протонного потенциала, функционирование АТФ-синтазы в качестве «протонной помпы» были изложены в 1961 году английским биохимиком Питером Митчеллом в выдвинутой им хемиосмотической гипотезе, ставшей сегодня общепризнанной теорией.
Интересно отметить, что синтез АТФ катализирует фермент АТФ-синтаза не только в митохондриях, но и в хлоропластах. При этом наблюдается сходство путей образования АТФ в этих органоидах.
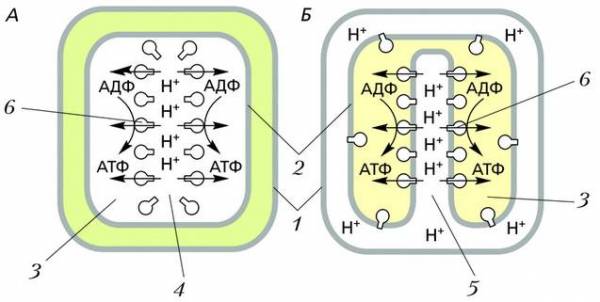 Поток протонов и синтез АТФ в тилакоидах хлоропласта (А) и в кристах митохондрии (Б): 1 – внешняя мембрана; 2 – внутренняя мембрана; 3 – матрикс (стрема); 4 – тилакоид; 5 – криста митохондрии; 6 – АТФ-синтаза
Поток протонов и синтез АТФ в тилакоидах хлоропласта (А) и в кристах митохондрии (Б): 1 – внешняя мембрана; 2 – внутренняя мембрана; 3 – матрикс (стрема); 4 – тилакоид; 5 – криста митохондрии; 6 – АТФ-синтаза
Перенос электронов по компонентам дыхательной цепи во внутренней мембране крист митохондрий подобен их транспорту по окислительной цепи в тилакоидной мембране хлоропластов. Высвобождаемая в этих процессах энергия и в том и в другом случае приводит к возрастанию разности протонного потенциала между матриксом (стромой) и межмембранным пространством органоидов (митохондрии или хлоропласта).